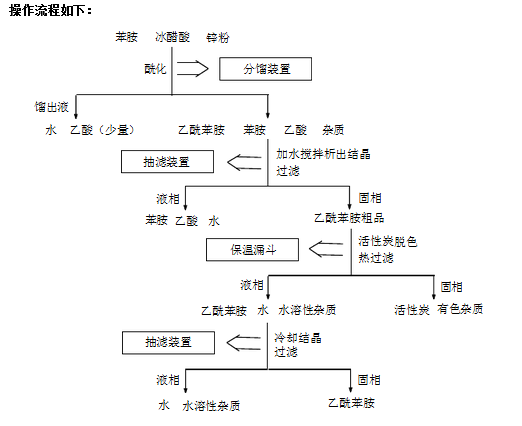
实验五 乙酰苯胺的制备(一)
一、实验目的
1.掌握苯胺乙酰化反应的原理和方法
2.掌握分馏的原理和操作
3.学习固体有机物的提纯方法??重结晶操作
二、实验原理
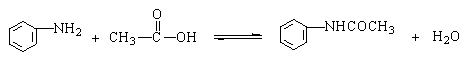
三、实验药品
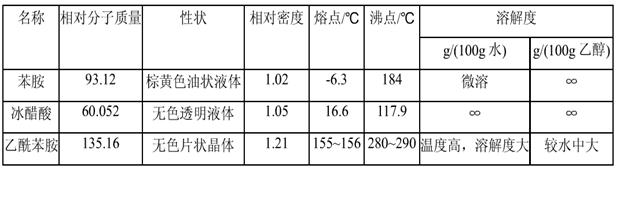
苯胺5mL(5.lg,0.05mol),冰醋酸7.4mL(7.8g 0.13mol),锌粉,活性炭。
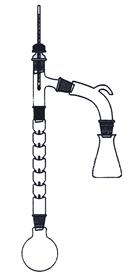
四、实验仪器
锥形瓶,分馏柱,蒸馏头,接引管,温度计。
五、实验步骤
在锥形瓶中放入5mL新蒸过的苯胺[1]、7.4mL冰醋酸和0.1g锌粉[2],小火加热至沸腾。保持温度计读数在105℃左右。经过40~60min,反应生成的水可以完全蒸出(含少量醋酸)。当温度计的读数发生上下波破动时(有时,反应器中出现白雾),反应即达终点,停止加热。
 在不断搅拌下将反应混合物趁热以细流慢慢倒入盛有100mL冷水的烧杯中。继续剧烈搅拌,并冷却烧杯,使粗乙酰苯胺成细粒状完全析出。用布氏漏斗抽滤析出的固体。用玻璃塞把固体压碎,再用5~10mL冷水洗涤以除去残留的酸液。把粗乙酰苯胺放入150mL热水中,加热至沸腾。如果仍有未溶解的油珠[3],需补加热水,直到油珠完全溶解为止[4]。
在不断搅拌下将反应混合物趁热以细流慢慢倒入盛有100mL冷水的烧杯中。继续剧烈搅拌,并冷却烧杯,使粗乙酰苯胺成细粒状完全析出。用布氏漏斗抽滤析出的固体。用玻璃塞把固体压碎,再用5~10mL冷水洗涤以除去残留的酸液。把粗乙酰苯胺放入150mL热水中,加热至沸腾。如果仍有未溶解的油珠[3],需补加热水,直到油珠完全溶解为止[4]。
稍冷后加入0.5g粉末活性炭[5],用玻璃棒搅动并煮沸1-2 min。趁热用保温漏斗过滤后用预先加热好的布氏漏斗减压过滤[6]。冷却滤液,乙酰苯胺成无色片状晶体析出。减压过滤,尽量挤压以除去晶体中的水分,再用少许冷水洗涤以除去残留的母液。产物放在表面皿上晾干后测定其熔点。
纯乙酰苯胺是无色片状晶体,熔点114℃。
附注
[1] 久置的苯胺色深,会影响乙酰苯胺的质量,所以应用新蒸过的苯胺。
[2] 锌粉的作用是防止苯胺在反应过程中被氧化。但必须注意,不能加得过多,否则在后处理中会出现不溶于水的氢氧化锌。新蒸过的苯胺也可以不加锌粉。
[3] 此油珠是熔融状态的含水的乙酰苯胺(83℃时含水13%)如果溶液温度在83℃以下,溶液中未溶解的乙酰苯胺以固体存在。
[4] 乙酰苯胺于不同温度在100mL水中的溶解度为:25℃,0.563g;80℃,3.5 g;100℃,5.2 g。本实验在重结晶时水的用量最好使溶液在80℃左右为饱和状态。
[5] 在沸腾的溶液中加入活性炭,会引起突然暴沸,致使溶液冲出容器。
[6] 事先将布氏漏斗及抽滤瓶应放在水浴中充分预热(不可直接在电热套上加热),否则乙酰苯胺晶体将在布氏漏斗及抽滤瓶内析出,引起操作上的麻烦和造成损失。
思考题
1.本反应为什么要控制分馏柱顶端温度在105℃?
2.合成乙酰苯胺时,锌粉起什么作用?加多少合适?
3.合成乙酰苯胺时,为什么选用分馏装置?
4.重结晶过程中,几种不同的杂质分别在哪一步被除去?
5.从苯胺制备乙酰苯胺时可采用哪些化合物作酰化剂?各有什么优缺点?
6.重结晶操作中,活性炭起什么作用?为什么不能在溶液沸腾时加入?
7.在制备乙酰苯胺的饱和溶液进行重结晶时,在杯下有一油珠出现,试解释原因。怎样处理才算合理?
第二篇:乙酰苯胺制备实验操作
乙酰苯胺的制备
目的和要求:
1苯胺乙酰化反应的原理和实验操作。
2.固体样品的制备。
3.分馏柱的原理和使用方法。
4.重结晶的方法及操作。
5.固体样品熔点的测定方法。
内容及原理:


乙酸与苯胺的反应较慢,且反应是可逆的,所以加过量冰醋酸提高产率,同时利用分馏柱将反应中产生的水从平衡中除去。
仪器和设备:
仪器:50ml烧瓶、分馏柱、温度计套管、温度计、冷凝管、尾接管、锥形瓶、布氏漏斗、抽滤瓶、安全瓶、抽滤装置、100ml烧杯、滤纸、天平、
试剂:5ml苯胺、7.5ml冰醋酸、少量锌粉、活性炭
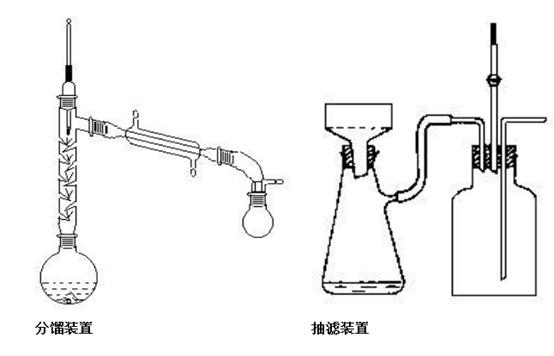
实验步骤:
1. 按图示组装装置、检查气密性。
2. 向分馏装置烧瓶中加入5ml苯胺、7.5ml冰醋酸、少量锌粉,通冷凝水,开始加热。
3. 待温度计示数稳定后又开始下降或烧瓶中出现白色雾气时停止加热,然后将烧瓶中的溶液倒入烧杯冷却结晶,然后抽滤,去其液。
4. 将得到的晶体用50ml蒸馏水煮沸,加入0.3g活性炭然后煮沸5-10分钟,趁热抽滤,取其液,冷却结晶。
5. 再次抽滤,到晶体,用少量水冲洗,冲洗时不断搅拌,然后抽干。
6. 将晶体取出,称重,计算产率。
理论产率:
苯胺摩尔数*(乙酸苯胺相对分子质量)=理论产量
产率=(纯品质量*70%/理论产量)*/100%
粗品颜色:暗黄色晶体
纯品颜色:白色晶体